我国科学家揭示铁死亡在肝纤维化发病机制中的关键机制
发布时间:2021-01-21 14:14:25 | 来源:【中国生物发展中心 2021年1月21日】
本文转自中国生物发展中心,转发仅为学习交流,若侵犯版权请联系小编删除。
肝纤维化是各种慢性肝病的共同病理过程,目前临床尚无有效的抗肝纤维化治疗药物。肝星状细胞(hepatic stellate cells, HSCs)活化是肝纤维化发生发展的核心环节,靶向诱导HSC死亡是防治肝纤维化的有效措施。铁死亡(Ferroptosis)是近年来发现的一种全新的细胞死亡方式,靶向诱导HSC铁死亡有望成为肝纤维化治疗的新策略。
2020年8月16日,我们科学家在国际著名期刊Autophagy杂志发表文章“RNA-binding protein ZFP36/TTP protects against ferroptosis by regulating autophagy signaling pathway in hepatic stellate cells”。首次揭示铁死亡在肝纤维化发病机制中的关键机制。
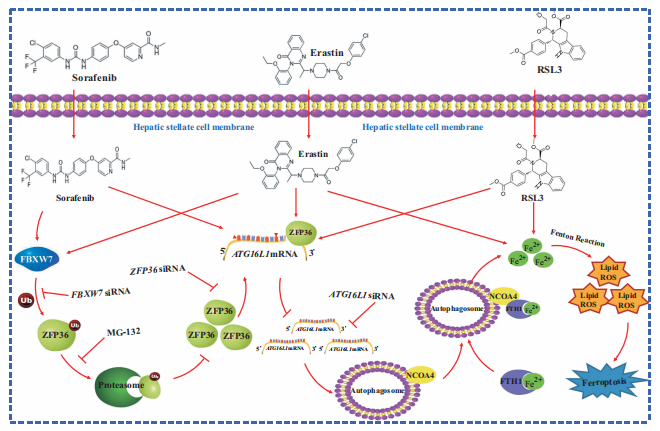
科研团队发现临床药物sorafenib以及临床前药物erastin能够靶向诱导活化型HSC发生铁死亡,且这一过程依赖于RNA结合蛋白ZFP36/TTP表达水平的下调。进一步的机制研究发现,sorafenib与erastin能够促进泛素化连接酶FBXW7靶向识别ZFP36蛋白氨基酸序列 “SFSGLPS”,诱导ZFP36发生泛素化降解,导致ZFP36蛋白表达水平降低。表达水平降低的ZFP36蛋白与自噬关键基因ATG16L1 mRNA 3’UTR中的“UUAUUUAUU”碱基序列特异性结合减少,使ATG16L1 mRNA更加稳定,促进ATG16L1蛋白表达,促进整体自噬水平,诱导NCOA4与FTH1结合,靶向降解储铁蛋白,过度释放铁离子,最终导致HSC铁死亡的发生。
该项工作主要创新点包括:首次明确泛素连接酶FBXW7靶向识别ZFP36蛋白氨基酸序列“SFSGLPS”,诱导ZFP36发生泛素化降解,对ZFP36在铁死亡中的翻译后修饰提出了新见解;首次明确RNA结合蛋白ZFP36通过影响自噬关键基因ATG16L1 mRNA稳定性调控HSC铁死亡进程,为进一步从转录后水平揭示铁死亡调控机制提供新的视角。
论文链接:https://doi.org/10.1080/15548627.2019.1687985